一个热门靶点的成药性出现突破,正在酝酿成为重磅炸弹。
10月13号,赛诺菲靶向OX40-配体单抗Amlitelimab在2b期试验STREAM-AD达成主要终点,可显著缓解中度到重度特应性皮炎成人患者的症状。凭借该项临床数据,Amlitelimab有望成为潜在“同类首创”靶向OX40-配体单抗。
10月12日,Astria Therapeutics宣布已与Ichnos Sciences达成许可协议,将开发OX40产品组合,交易条件包括1500万美元首付和潜在3.05亿美元里程碑,用于治疗特应性皮炎和其他过敏性amp;免疫性疾病。
OX-40靶点的热度在提升,但也并非一朝一夕之功。在肿瘤领域,辉瑞、罗氏的OX-40激动剂因疗效不佳而失败,百时美施贵宝、GSK、阿斯利康同样有类似遭遇,现有进入临床后期安进、赛诺菲的OX-40抗体,均在自免取得突破。
安进、赛诺菲的OX-40分子,全部源自于外购。2021年6月,安进以4亿美元首付款和8.5亿美元的里程碑付款从协和麒麟引进Rocatinlimab;赛诺菲的Amlitelimab原本由Kymab研发,2021年11月赛诺菲以14.5亿美元收购了Kymab。
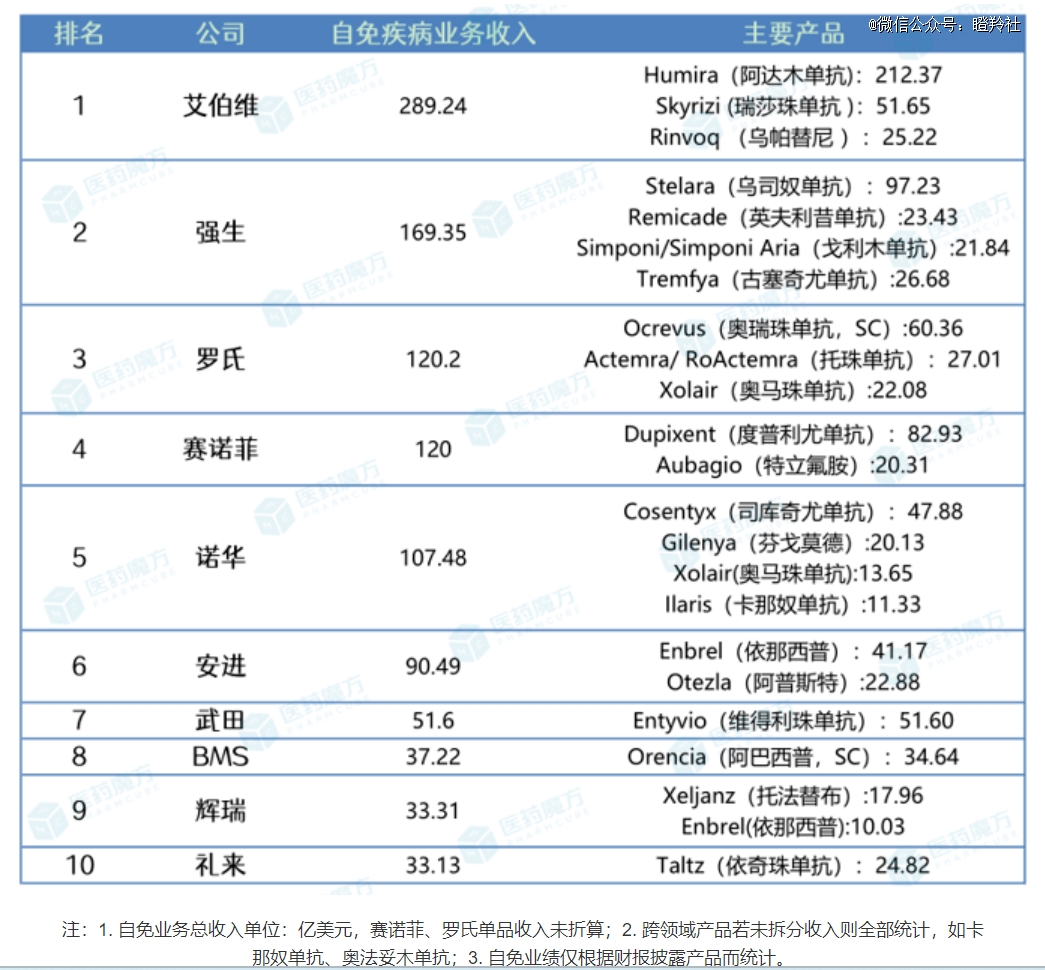
在2022年全球自免领域制药巨头TOP10的排名中,赛诺菲和安进分别排名第四和第六,两者曾产出像度普利尤单抗、依那西普这样的重磅炸弹,这也给两者共同下重注OX-40靶点的前景增添了更多色彩。
01OX-40,肿瘤和自免领域的多面手
OX40是一个属于肿瘤坏死因子受体超家族(TNFRSF)的细胞表面蛋白,主要在活化的T细胞上表达。
曾有人将PD-1抗体等免疫检查点抑制剂的作用喻为“去掉抑制免疫系统的刹车”,而将OX-40抗体等刺激免疫反应疗法喻为“踩下免疫系统的油门”。众所周知,T细胞的激活是机体免疫应答的核心,从上述这段比喻中看出,OX-40在调节T细胞的活动和生存方面,起到重要作用。
OX40本身的独特机制,决定了其广阔的市场潜力,及研发者对其开发策略的多样性。如OX40可以广泛地抑制多种疾病相关信号通路,能够在多种适应症中展露治疗潜力;再如OX40可以抑制记忆T细胞,往往在停药后病人还能持续应答。
目前,全球OX40的研发方向主要聚焦在肿瘤、自免两大领域。
在肿瘤领域,OX40与OX40L共刺激信号进行肿瘤治疗是最主要的研究方向之一,研发管线多为OX40激动剂;其主要原理是OX40信号的传导可以促进常规CD4+和CD8+T细胞存活,增加细胞因子如IL-2、IL-4、IL-5的表达,增强肿瘤特异性效应T细胞免疫反应,从而起到灭杀肿瘤细胞作用。
值得注意的是,OX40在多种不同肿瘤组织中的浸润性淋巴细胞表面均有表达,包括乳腺癌、黑色素瘤、B细胞淋巴瘤和头颈癌等,可探索的适应症市场天花板很高;同时,免疫检查点抑制剂与靶向共刺激受体的组合疗法也成为时下的热门探索方向,不仅帮助肿瘤患者去掉刹车,还要踩下油门,强化对肿瘤的杀伤效果。
在自免领域,药物主要研发方向为OX40或其配体OX40L的抗体,通过阻断OX40与OX40L的结合改善自身抗原特异性T细胞反应,并降低自免疾病中的免疫活性。
OX40作为上游调控蛋白,可调节多种异常活化的病理性T细胞的增殖、活化、记忆形成,可对Th1/Th2/Th17/Th22等多种T细胞介导炎症应答的起始和放大进行抑制。
由此,可以解释OX40抗体为何在治疗特应性皮炎、斑秃、类风湿关节炎、银屑病关节炎、移植物抗宿主病、哮喘等等多个适应症中都具备一定潜力。
02在特应性皮炎领域,OX40率先绽放光芒
无论是赛诺菲的OX40L抗体Amlitelimab还是安进的OX40抗体,均率先在特应性皮炎适应症上取得突破性进展。
鉴于目前IL-4Rα抗体在特应性皮炎所展现出的强势,市场必定会将赛诺菲的Amlitelimab数据与之进行对比。
我们不妨以特应性皮炎常用的两大终点:总体评估评分和皮损消退面积≥75%(EASI-75),对Amlitelimab和Dupilumab(赛诺菲达必妥)进行非头对头的比较(不同临床基线不同,仅供参考)。
IGA评分层面,Amlitelimab治疗组22.1%和45.5%患者在第16周和第24周达到 IGA 0/1,而安慰剂组患者达到IGA 0/1对应比例为5.1%和11.4%;而Dupilumab两项临床的16周数据相比安慰剂组分别是38%对10%、36%对9%;纸面上看,Amlitelimab数据略逊于Dupilumab。
EASI-75评分层面,Amlitelimab治疗组分别有40.3%和54.5%患者在第16周和第24周达到大于75%的皮损消退面积,对应安慰剂组的比例为11.4%和17.7%;在Dupilumab的16周数据中,其对安慰剂的EASI-75数据分别为51% vs 15%、44% vs 12%;剔除掉安慰剂的影响,两者在该数据角度效力相仿。
还值得注意的是,在一些问题上,OX-40抗体相比IL-4Rα抗体给出了更优解。
瘙痒伴随着几乎所有特应性皮炎患者,而且越挠越痒,这主要是由Th2细胞产生的一些细胞因子刺激皮肤产生IL-31(瘙痒因子)。IL-31不仅主引起瘙痒,而且用手挠会加重炎症反应,同时又促进IL-31的表达,如此循环的结果就是越挠越痒。
IL-4Ra作为下游通路,相关抑制剂并不能很好解决这个问题。而OX-40作为T细胞二级共刺激信号,可阻断两者的相互作用调控Th1/Th2/Th17/Th22通路,从而一定程度可以解决特应性皮炎的瘙痒问题。安进Rocatinlimab的IIb期临床数据,就在NRS这一指标上展现出优于Dupilumab的潜力。
另外,基于前文叙述的OX40可抑制记忆T细胞的机理,我们可以看到如Rocatinlimab、Amlitelimab和Telazorlimab等OX-40相关分子的临床研究中,大多数特应性皮炎患者在停药4个月甚至半年后均能维持较好的治疗效果,有着长效缓解的优点,同时不额外增加安全性问题。
03国内OX40的热烈战争
看似国内创新药企们在OX-40热闹非凡,实则几乎可以看到几乎9成以上的布局适应症为肿瘤。
在OX-40靶点布局上,信达生物的IBI-101在2019年2月率先进入临床,主要作用机制走的是激动剂的路线,旨在增强效应T细胞的活化,并介导调节性T细胞的清除,从而起到抑制肿瘤细胞生长的作用;另外,当时还有一款OX40/PD-L1双抗IBI-327处于临床前阶段;但在最新2023年公司中报中,这两条管线已经找不到了,大概率是进展不顺利而被优化。
另一个较强大的*者是百济神州的BGB-A445,据资料显示,BGB-A445与其他大部分在研OX40抗体存在差异,其不通过阻断OX40/OX40L结合发挥作用;2023年百济神州中报显示:BGB-A445联合替雷利珠单抗探索实体瘤治疗的临床已经推进到二期,算是当下国内进度最快的OX40抗体之一。
国内通过研发OX-40靶点开发自免适应症的Biotech几乎少得可怜,目前已披露*进入临床阶段的分子是和黄医药和创响生物开发的IMG-007,是一种人源化IgG1单抗,可特异性地结合OX40受体并阻断OX40与OX40L之间的信号传导,特点是具有超长半衰期和没有抗体依赖性细胞介导的细胞毒性效应,目前IMG-007正通过一起临床探索其在AD领域的安全性和更低给药频率的效果。
整体来看,虽然有大量管线处于临床阶段,国内OX-40抗体对自免大适应症的开发仍存在较大差异化机会。
结语:OX-40这个新兴靶点正在悄悄地在肿瘤之外的领域绽放光芒,这可能是大部分当年做OX-40肿瘤适应症me-too的Biotech没有想到的。可惜的是,OX-40对于肿瘤和自免治疗机制的不懂,造成了如今的空白地带。


















